近日,金河生物发布公告,宣布中止非洲猪瘟冻干灭活疫苗的研发与申报工作。这一决定是公司经审慎评估后的战略止损,也让其历时8年布局的非洲猪瘟疫苗研发项目就此止步,而与此同时,行业内其他科研机构和企业的非洲猪瘟疫苗研发却取得重要突破,行业研发格局呈现出明显分化。

金河生物:专利谈判僵局成直接诱因多重因素致战略止损
金河生物此次中止非洲猪瘟冻干灭活疫苗研发,直接原因在于核心的专利许可环节陷入僵局。公告显示,其控股子公司吉林佑本开展非洲猪瘟灭活疫苗研发,需与专利转让方签订《技术许可(专利权)合同》,这是获取生产用毒和检验用毒的关键前提,但多方就合同关键条款始终无法达成一致,直接导致项目研发进度丧失确定性。
除专利许可的直接阻碍外,非洲猪瘟疫苗研发本身的行业特性,也是金河生物作出止损决定的重要原因。非洲猪瘟疫苗研发被公认为世界性难题,技术门槛远高于普通疫苗,且监管审批周期漫长,资金成本持续累积,即便研发成功,商业化落地和业绩兑现仍存在较大不确定性。
同时,金河生物选择的冻干灭活疫苗路线本身存在先天技术挑战,非洲猪瘟病毒结构复杂,灭活过程中极易破坏其保护性抗原,进而导致疫苗免疫原性不足,这也为研发工作增添了技术难度。此次研发中止也给金河生物带来了直接的财务影响,公司基于会计准则谨慎性原则,对收购吉林佑本形成的商誉计提减值准备约1.75亿元,计提后该商誉账面净值归零。
金河生物的非洲猪瘟疫苗研发布局,核心依托于对吉林佑本的收购,此次收购初衷是为了拓展公司在非洲猪瘟防控及疫苗产研领域的布局,提升疫苗产研转化速度,进一步扩大其在动物疫苗领域的市场占有率。
而其研发筹备工作的推进,始于农业农村部的相关评审意见。2023年7月,农业农村部畜牧兽医局指出,其非洲猪瘟疫苗中试单位的生产和检验等条件不符合要求,为此,吉林佑本和金河佑本分别启动了生产车间、检验动物房等设施的生物安全三级防护升级与资质验收工作。
此后,公司按计划完成了一系列硬件升级和资质验收:2025年1月25日,吉林佑本疫苗生产车间通过生物安全三级防护检查验收;2025年7月27日,金河佑本检验用攻毒动物房及其活毒废水处理设施及防护措施完成同级别验收;2025年8月28日,金河佑本顺利通过兽药GCP猪安全性试验和猪有效性试验项目增项验收。截至2025年第三季度末,金河生物已具备开展非洲猪瘟疫苗临床试验的全部硬性条件,疫苗申报所需的生产、检验设施及临床试验资质均达标,研发工作看似到了“临门一脚”的阶段,却因专利许可这一“软件”问题最终止步。
哈兽研非瘟疫苗对妊娠母猪安全,不影响仔猪生长
近日,中国农业科学院哈尔滨兽医研究所关于非洲猪瘟基因缺失减毒活疫苗HLJ/18-7GD株对妊娠母猪安全性的临床试验研究在《新兴微生物和感染(Emerging Microbes & Infections)》发表。研究结果证实,非洲猪瘟基因Ⅱ型减毒活疫苗(HLJ/18-7GD株)对妊娠母猪及其仔猪安全。
非洲猪瘟持续威胁全球生猪产业。近年来,多款基因缺失减毒活疫苗陆续进入临床试验,部分已在东南亚国家获批使用于育肥猪。鉴于弱毒活疫苗无法避免外溢传播至母猪,系统评估活疫苗对母猪及其仔猪的健康与生产性能影响至关重要。
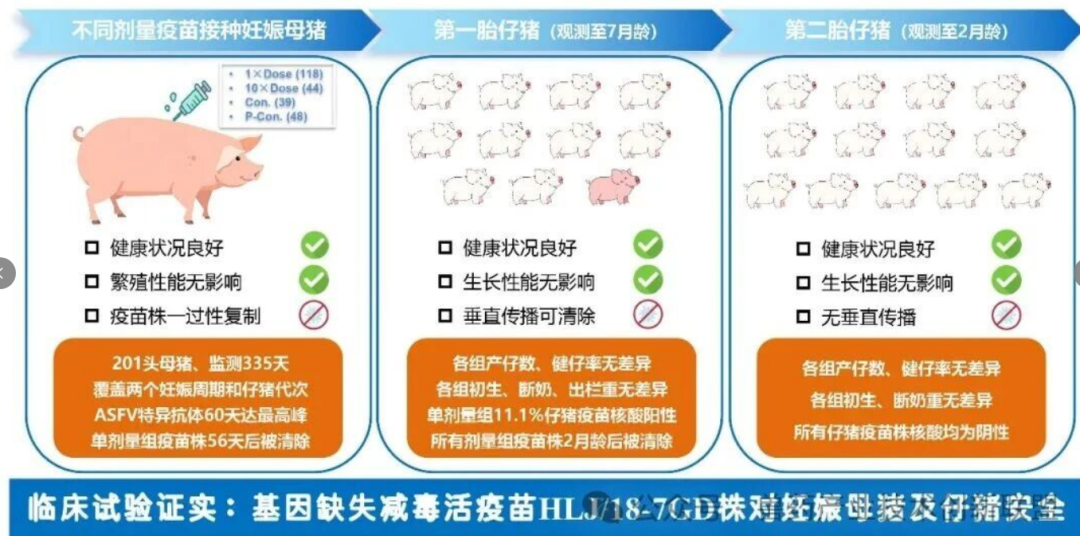
前期实验室研究初步证实,HLJ/18-7GD株对育肥猪和母猪安全,对同源基因Ⅱ型强毒株提供有效保护。为深入评估该疫苗对繁殖母猪的安全性,按照农业农村部批准试验方案,选择了一家典型小型繁殖母猪养殖场,在严格生物安全受控条件下,对HLJ/18-7GD株进行了系统的安全性研究。试验入组妊娠能繁母猪共201头,分为三个组,分别为单剂量组(106.2TCID50)、10倍剂量组(107.2TCID50)及未接种对照组。疫苗接种后持续观察335天,跨越连续两个胎次。同时,随机选取不同组试验母猪分娩第一胎断奶仔猪共219头,育肥观测至7月龄。
结果显示,HLJ/18-7GD株对妊娠母猪具有良好的安全性,接种后母猪无发热、无非洲猪瘟相关慢性和急性临床症状;有关繁殖与生产性能指标,包括妊娠期、分娩率、受孕率、产仔率,以及分娩仔猪健仔率、初生重、断奶重、生长发育、育肥增重、出栏重,三个试验组间无明显差异,试验场与平行场间也无明显差异。
HLJ/18-7GD株在妊娠母猪及其生产第一胎少部分仔猪体内呈阶段性低水平复制,单剂量组母猪在接种56天后被清除,10倍剂量组母猪在接种84天后被清除;疫苗毒垂直传播能力低,单剂量组仅有11.1%的第一胎仔猪体内检测到疫苗毒核酸阳性,且在2月龄内被完全清除,第二胎仔猪体内均未检测到疫苗毒核酸阳性。
该研究通过系统的田间试验,以详实的数据证明了非洲猪瘟基因缺失减毒活疫苗HLJ/18-7GD株生物安全性良好,对母猪及其后代仔猪的健康和生产性能均无不良影响,具有生产应用潜力。
生物股份:全球首款非瘟亚单位疫苗取得关键突破
近日,金宇生物技术股份有限公司(简称“生物股份”)宣布,其联合攻关的非洲猪瘟(ASF)亚单位疫苗已完成首轮临床试验攻毒验证,保护率达到评价标准。这标志着我国在攻克这一全球养猪业百年难题上,取得了从“0到1”的关键性突破。
自2018年传入我国以来,非洲猪瘟给养殖业造成了巨大经济损失,成为产业高质量发展的关键瓶颈。由于病毒结构复杂,全球范围内长期缺乏安全有效的商业化疫苗。
生物股份自2019年起联合中国科学院生物物理所等单位启动攻关,历时7年,累计投入近6亿元,并行探索多条技术路线。最终,基于对安全性、有效性和产业化前景的综合考量,公司聚焦于基因工程亚单位疫苗路线,并成功于2025年7月获得农业农村部临床试验批件。
2025年10月份,生物股份在内蒙古、湖北、河北、甘肃四省五家规模化猪场启动临床试验,共选择11005头实验用猪,其中疫苗免疫组10035头,安慰剂组及对照组970头。2026年1月份,首轮攻毒实验圆满结束。生物股份研发总监李劼表示,实验采用基因Ⅱ型强毒株HB19,通过口腔喷雾方式攻毒,剂量为8000HAD50。结果显示:免疫组在28天攻毒结束后均健活,保护率达到评价标准要求;而对照组在28天内全部发病并死亡,死亡率为100%。
尤为关键的是,该疫苗采用基因工程亚单位技术,仅表达8个保守抗原蛋白,不含活病毒,彻底杜绝了毒力返强风险。同时,其靶点在当前流行的重组毒株中同源性高达99.7%。生物股份总裁张竞表示:“公司依托高级别生物安全实验室(ABSL-P3)优势,建立了高通量分子筛选平台,完成了100多个非洲猪瘟靶点蛋白的AI筛选与合成表达、攻毒验证选,积累了大量数据,让我们在应对新型毒株上有坚实的技术基础。”
【版权说明】猪博士平台转载的文章均已注明来源、猪博士平台原创文章其他平台转载须注明来源,特别说明的文章未经允许不可转载。我们发布的文章仅供养猪人学习参考,不构成投资意见。如有不妥,请联系客服删除




发表评论 取消回复